Sélectivité des mâles pour leurs partenaires chez la sauterelle Ephippiger diurnus et facteurs extrinsèques l’influençant en conditions naturelles.
Alicia COLIN-JARRIGE
Institut de Recherche sur la Biologie de l’Insecte (IRBI UMR 7261)
Université François Rabelais, Parc Grandmont, 37200 Tours
Email : alicia.colin (at) etu.univ-tours.fr
Résumé
Tout comme la sélection naturelle, la sélection sexuelle est un important moteur d’évolution des espèces. Bien que la vision classique de la sélection sexuelle oppose des femelles sélectives à des males compétitifs, il apparait de plus en plus évident que les mâles choisissent aussi leurs partenaires sexuels, notamment chez les espèces ou l’investissement reproducteur du mâle est important. Or, si le choix des mâles par les femelles a fait l’objet de nombreuses études théoriques et empiriques, le choix des femelles par les mâles reste moins étudié, notamment au sein d’espèces où les deux sexes sont sélectifs. Chez Ephippiger diurnus, une sauterelle de la famille des Tettigoniidae retrouvée dans tout le pourtour Méditerranéen, les mâles transfèrent pendant l’accouplement des nutriments aux femelles sous la forme d’un large spermatophore. La production d’un spermatophore étant couteuse en temps en énergie, les mâles doivent attendre en moyenne 90 h après le transfert d’un tel cadeau nuptial avant d’être en mesure de s’accoupler de nouveau. On peut donc s’attendre à ce qu’un tel investissement prédispose les mâles à être sélectifs au regard des partenaires sexuelles rencontrées. Allant dans ce sens, de précédentes études menées au laboratoire ont montré que les mâles pouvaient être sélectifs sous certaines circonstances, en favorisant la taille et/ou la qualité du spermatophore au regard de la femelle rencontrée. C’est la raison pour laquelle nous avons souhaité étudier cette sélectivité et les facteurs extrinsèques qui l’influencent en conditions naturelles. L’étude s’est déroulée sur deux périodes au cours de l’été 2013, au Col de Mantet dans les Pyrénées Orientales. Sur place, nous avons estimé le ratio de mâles et de femelles présents et sexuellement réceptifs (Sexe Ratio et Sexe Ratio Opérationnel), ainsi que la qualité des femelles disponibles, ces trois paramètres ayant été identifiés comme d’importance dans la mise en place du choix mâle chez d’autres espèces. Enfin, nous avons estimé le taux de sélectivité des mâles aux travers de tests comportementaux in situ. Les résultats obtenus au cours de cette campagne de terrain révèlent une importante variabilité dans la qualité des femelles disponibles (statut reproducteur vierges/accouplées, nombre d’œufs présents dans les ovaires…), ainsi qu’un sexe ratio opérationnel extrêmement biaisé en faveur des mâles. Ceci signifie que peu de femelles sont sexuellement réceptives au vu du nombre de mâles sexuellement actifs. Sous ces conditions particulières, il n’est pas attendu que ces derniers se montrent sélectifs mais au contraire saisissent chaque opportunité d’accouplement se présentant à eux indépendamment de la qualité de la femelle rencontrée. En effet, les résultats des tests de sélectivité des mâles ne suggèrent pas d’ajustement de la qualité du spermatophore au regard de la qualité de la femelle rencontrée et ce au cours des deux périodes étudiées.
Justification
Tout comme la sélection naturelle, la sélection sexuelle est un important moteur d’évolution des espèces, notamment en ce qui concerne l’évolution des soins parentaux et des caractères sexuels secondaires [1]. Classiquement, lors de l’appariement, les mâles entrent en compétition pour l’accès aux femelles, tandis que ces dernières choisissent parmi les différents partenaires potentiels [1]. Ces rôles sexuels conventionnels, opposant femelles sélectives et mâles compétitifs, trouveraient leur origine dans l’asymétrie d’investissement reproducteur selon le sexe [2]. En l’occurrence, la reproduction serait plus couteuse pour les femelles, tout d’abord en ce qui concerne la production des gamètes, mais aussi les soins apportés aux jeunes [3]. Il en résulterait un taux de reproduction potentiel plus faible pour les femelles, ces dernières représentant alors le sexe « rare » dont la disponibilité conditionne le succès reproducteur des mâles [4].
Toutefois, il semble de plus en plus évident que l’appariement peut être coûteux pour les mâles. Par exemple, le transfert de substances accessoires conjointement à l’éjaculat peut représenter un coût important et réduire considérablement le potentiel reproducteur des mâles [5]. C’est notamment le cas lorsque les mâles transfèrent un cadeau nuptial aux femelles, tel que le spermatophore produit par de nombreux orthoptères. Un tel investissement devrait engendrer une certaine sélectivité des mâles envers leurs partenaires sexuels [6]. Or, si les choix des mâles par les femelles ont fait l’objet de nombreuses études théoriques et empiriques [1] le choix des femelles par les mâles a été bien moins étudié, en particulier chez les espèces où les deux partenaires montrent un certain degré de sélectivité (choix de partenaire mutuel). Et, en particulier, les données de terrain sont anecdotiques [7].
Aussi, notre étude avait pour objectif de caractériser le choix des mâles ainsi que les facteurs extrinsèques impliqués dans cette sélectivité en conditions naturelles, chez la sauterelle Ephippiger diurnus (Orthoptère).
Chez cette espèce, les mâles se regroupent en chorus et produisent un chant par stridulation [8], vers lequel s’orientent les femelles sexuellement réceptives (phonotaxie). De précédentes études indiquent que les femelles choisissent les mâles sur la base de leur chants [9]. A l’issue de l’accouplement, le mâle transfère un spermatophore pouvant atteindre chez cette espèce jusqu’à 40 % du poids du mâle [10], comportant une large partie qui est ingérée par les femelles. Après transfert d’un spermatophore, les mâles présentent une période réfractaire d’en moyenne 90 h au cours de laquelle ils ne chantent ni ne peuvent se ré-accoupler [16]. Aussi, cet investissement est couteux en temps et en énergie et prédispose les mâles à être, eux aussi, sélectifs. De précédentes études menées au laboratoire vont en ce sens et suggèrent que les cadeaux nuptiaux transférés par les mâles varient au regard du poids et de l’âge des femelles rencontrées [11].
En conditions naturelles, de nombreux facteurs peuvent influencer l’intensité de la sélectivité des mâles. Tout d’abord, la variance dans la qualité des femelles disponibles, telles que les différences dans leur statut reproducteur, leur âge, ou leur taux de fécondité. En effet, plus les femelles sont de qualité variable, plus les bénéfices potentiels à être sélectif sont grands [12]. Par exemple, chez de nombreux insectes, la taille corporelle de la femelle est souvent corrélée à sa fécondité, une affirmation qui s’avère être vérifiée chez Ephippiger diurnus [16]. Dans ce cas, les mâles qui favorisent les femelles les plus grosses seront avantagés [13]. Ensuite, le statut reproducteur (vierge ou déjà accouplée) des femelles peut également avoir des conséquences sur le succès reproducteur des mâles, notamment chez les espèces où la fécondité des femelles décroit avec le nombre d’accouplements, ou encore lorsqu’il existe de la compétition spermatique [14]. Aussi, les mâles devraient préférer les femelles vierges [15]. Enfin, le Sexe Ratio Opérationnel (SRO), correspondant au nombre de femelles sexuellement disponibles par rapport au nombre de mâles sexuellement disponibles peut conditionner la direction de la sélectivité : si les femelles sont plus nombreuses que les mâles, on peut s’attendre à ce que ces derniers soient plus sélectifs que dans le cas inverse [15]. Par ailleurs, l’ensemble de ces facteurs peuvent être fortement variables au cours de la saison de reproduction des insectes.
Le projet de terrain visait trois objectifs principaux :
- Estimer le sexe ratio, le sexe ratio opérationnel (SRO) ainsi que la qualité des femelles disponibles (en termes de poids et de statut reproducteur).
- Evaluer l’évolution de ces facteurs extrinsèques (SRO, variance de qualité des femelles) au cours de la saison.
- Caractériser l’évolution de la sélectivité des mâles en fonction de celle des paramètres précédents en conditions naturelles.
Méthodes
Le lieu choisi pour l’étude se situe au Col de Mantet dans les Pyrénées Orientales (latitude 42,5°N, longitude 2,3°E), à 1700 m d’altitude. Dans le but d’évaluer l’évolution des différents paramètres étudiés au cours de la saison de reproduction des insectes, le projet s’est déroulée sur deux périodes : du 12 au 23 Aout 2013 puis du 12 au 24 Septembre 2013.
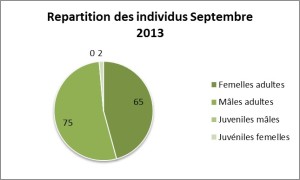
Mesure du sexe ratio : Nous avons délimité 33 quadrats (15 en Aout et 18 en Septembre) de 5 ,20 x 5,20 m au sein desquels l’ensemble des individus a été prélevé. Au sein de chaque quadrat, le nombre d’individus (adultes et juvéniles) ainsi leur sexe a été noté.
Mesure du sexe ratio opérationnel : La mesure du SRO a été réalisée en considérant les individus prélevés au sein de chacun des 33 quadrats. La réceptivité des mâles a été évaluée en dénombrant les mâles chanteurs par observation le lendemain du jour de leur capture (un mâle chanteur est un mâle sexuellement réceptif). La réceptivité sexuelle des femelles a été évaluée en mesurant leur réponse phonotactique au chant de mâles diffusés à l’aide d’un haut-parleur également le lendemain du jour de capture (cette méthode a déjà été testée et utilisée avec succès au laboratoire en 2012).
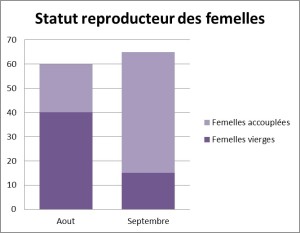
Estimation de la qualité des femelles disponibles : Environ la moitié des femelles prélevées dans les quadrats ont été pesées puis disséquées. Le nombre et la maturité des œufs présents dans les ovaires ont été compté (la maturité des œufs peut être déterminée sur la base de leur coloration). Le statut reproducteur des femelles a été déterminé par examen visuel de la spermathèque (translucide lorsque les femelles sont vierges et orange opaque lorsqu’elles sont accouplées).
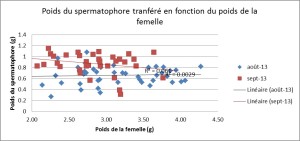
Mise en évidence de la sélectivité des mâles: La sélectivité des mâles a été évaluée à l’aide de tests d’accouplements en conditions contrôlées. Les mâles ont été placés en situation de choix entre femelles sexuellement réceptives de poids différents. A la suite d’un accouplement, le spermatophore est prélevé puis pesé de sorte à quantifier l’investissement reproducteur des mâles et déceler d’éventuels ajustements au regard de la qualité de la femelle. Les femelles réceptives utilisées lors de ces tests ont été obtenues par capture et isolement dans des boites individuelles de femelles capturées sur le terrain, hors des zones délimitées par les quadrats. Chaque jour à partir du lendemain de la date de leur capture, leur réceptivité sexuelle a été testée selon la méthode décrite plus haut (cf. Mesure du sexe ratio opérationnel), permettant de n’utiliser pour tester la sélectivité des mâles que des femelles elles-mêmes sexuellement réceptives.
Résultats et discussion
Mesure du sexe ratio :
Au total, 312 individus ont étés collectés sur l’ensemble des 33 quadrats, dont 172 en Aout et 140 en Septembre. Il n’y a pas de différence significative dans l’abondance relative des sexes entre les deux périodes (Chi-deux, 0,812, 1 ddl, p=0,367).
Mesure du sexe ratio opérationnel :
- Réceptivité sexuelle des femelles : La réceptivité sexuelle des femelles s’est avérée extrêmement faible au cours des deux périodes : en Aout seulement 4,29 % des femelles testées se sont dirigées vers un chant de mâle diffusé à l’aide d’un haut-parleur (3 sur 70 femelles testées). En Septembre, 4,62 % des femelles (3 femelles sur 65 testées) se sont avérées sexuellement réceptives.
- Réceptivité sexuelle des mâles: Au mois d’Aout, 58,8 % des mâles chantaient le lendemain de leur capture, contre 52 % en Septembre. Ces chiffres nous permettent d’estimer un sexe ratio opérationnel très biaisé en faveur des mâles de 13,73 en Aout et 11,27 en Septembre, signifiant qu’en moyenne, une femelle est sexuellement réceptive pour 13,73 mâles en Aout, tandis qu’une femelle est sexuellement réceptive pour 11,27 mâles en Septembre.
Estimation de la qualité des femelles disponibles : La qualité des femelles varie fortement au cours de la période étudiée, notamment en ce qui concerne le statut reproducteur : 66,7 % des femelles sont vierges en Aout, contre seulement 23 % des femelles en Septembre. Par ailleurs, le nombre d’œufs ainsi que le poids des femelles augmente significativement au cours de la saison de reproduction (t=2,49, 77 ddl, p=0,015, voir ci-dessous).
Mise en évidence de la sélectivité des mâles:
Les tests d’accouplement en condition contrôlées révèlent une forte corrélation entre le poids du spermatophore transféré aux femelles et le poids du mâle, (p<0,0001, r=0,65, n=79). De plus, les mâles transfèrent des spermatophores significativement plus gros en Septembre (t=-5,21, 77 ddl, p <0,001), bien qu’il n’existe pas de différence dans le poids des mâles entre les deux périodes (t =-1,30, 77 ddl, p=0,195). En revanche, la taille du cadeau nuptial transféré par les mâles est indépendante de la taille de la femelle, ce qui suggère que les mâles n’ajustent pas leur spermatophore au regard de la taille de la femelle rencontrée
Nos résultats révèlent d’importants contrastes dans la qualité des femelles, que ce soit au cours d’une même période qu’entre Aout et Septembre. Sous ces conditions, les mâles pourraient tirer avantage à être sélectifs et maximiser leur succès reproducteur en favorisant les femelles de meilleure qualité, notamment les plus grosses qui présentent une meilleure charge en œufs. Toutefois, tout au long de l’étude, le sexe ratio opérationnel s’est avéré extrêmement baisé en faveur des mâles, indiquant que les probabilités pour qu’un mâle rencontre une femelle sexuellement réceptive sont faibles. Dans ce cas, il n’est pas attendu que ces derniers se montrent sélectifs mais au contraire saisissent chaque opportunité d’accouplement se présentant à eux, et ce indépendamment de la qualité de la femelle rencontrée. Les résultats des tests de sélectivité des mâles vont dans ce sens et ne suggèrent pas d’ajustement de la qualité du spermatophore au regard du poids de la femelle rencontrée.
[1] Andersson, M. 1994. Sexual selection. Princeton, UK: Princeton University Press.
[2] Bateman AJ, 1948. Intra-sexual selection in Drosophila. Heredity 2: 349-368.
[3] Williams, G.C. 1966. Adaptation and Natural Selection. A Critique of Some Current Evolutionary Thought. Princeton University Press, Princeton.
[4] Clutton-Brock TH, Vincent AC. 1991. Sexual selection and the potential reproductive rates of males and females. Nature 351: 58–60
[5] Vahed, K. 1998. The function of nuptial feeding in insects: review of empirical studies. Biological Reviews, 73, 43-78.
[6] Edward, D. A., Chapman T. 2011. The evolution and significance of male mate choice. Trends in Ecology and Evolution, 29, 647-654.
[7] Forsgren, E., Amundsen, T., Borg, A. and Bjelvenmark, J. 2004. Unusually dynamic sex roles in a fish. Nature 429, 551-554.
[8] Dumortier, B. 1972. Photoreception in the carcadian rhythm of stridulatory activity in Ephippiger (Ins., Orthoptera). Likely existence of two photoreceptive systems. Journal of comparative physiology 77:11-80.
[10] Wedell, N. 1994. Variation in nuptial gift quality in bushcrickets (Orthoptera:Tettigoniidae). Behavioral Ecology, 5, 418-425.
[11] Colin, A., Greenfield, M.D., Goubault, M. 2013. Male song as a predictor of the nuptial gift in bushcrickets: on the confounding influence of male choice. Animal Behaviour, 85, 1427-1434.
[12] Parker, G.A. 1983. Mate quality and mating decisions. In Mate Choice (Bateson, P.P.G., ed.), pp. 141–166, Cambridge University Press
[13] Dosen, L.D. and Montgomerie, R. 2004. Female size influences mate preferences of male guppies. Ethology 110, 245–255
[14] Simmons, L. W. 2001. Sperm Competition and Its Evolutionary Consequences in the Insects. Princeton, UK: Princeton University Press
[15] Bonduriansky, R. 2001. The evolution of male mate choice in insects: a synthesis of ideas and evidence. Biological Review of the Cambridge Philosophical Society, 76, 305-339
[16] Colin, Alicia, 2012, données non publiées.








très intéressant. surtout la méthodologie appliqué pour la détermination des sexes ratio