La proline, vecteur des interactions plantes-insectes ? Cas de deux espèces envahissantes, Lasius neglectus et Fallopia sp.
Loïc Teulier
Laboratoire d’Ecologie des Hydrosystèmes Naturels et Anthropisés
UMR 5023 CNRS – UCB Lyon 1
Bâtiment Raphaël Dubois – Campus de la Doua
43, bvd du 11 novembre 1918
F-69622 Villeurbanne cedex
loic.teulier (at) univ-lyon1.fr
Résumé
Aux vues du nombre de publications portant sur le sujet, la richesse et la diversité des mécanismes participant aux interactions plantes-insectes présentent des possibilités d’investigation exceptionnelles. Dans le but de caractériser plus particulièrement le rôle de la proline, acide aminé potentiellement utilisé comme substrat énergétique dans une interaction entre deux espèces invasives, la renouée du Japon (Fallopia sp.) et une fourmi (Lasius neglectus; Fig. 1), nous nous sommes intéressés dans un premier temps à tester expérimentalement notre hypothèse, selon laquelle, les fourmis préfèrent une solution sucrée lorsqu’elle est supplémentée en proline.
Pour se faire, après avoir prélevé une colonie de Lasius neglectus, nous les avons gardé en conditions contrôlées et standardisées afin d’obtenir de petites colonies d’environ 500 individus. Ces différentes sous-colonies nous ont permis de générer un ensemble de tests de préférences en « Y » pour caractériser la capacité de choix entre des solutions sucrées supplémentées ou non en proline ou en alanine (un autre acide aminé, présent également dans le nectar extra-floral).
Suite à cette série d’expériences, nous n’avons pu discriminer statistiquement les différentes solutions supplémentées en acides aminés. Cependant cette première expérience nous a permis de mettre au point le protocole expérimental, notamment de suivi vidéo, et de stabulation des différentes colonies de fourmis.
Justifications
Les interactions plantes-insectes, pourtant très bien décrites dans la littérature, constituent toujours le sujet de nombreuses études scientifiques, tant l’importance et la diversité des mécanismes qui entrent en jeux sont difficiles à appréhender. Un des acteurs majeurs de ces interactions est sans doute le nectar, source de sucres et d’acides aminés produit par la plante particulièrement appréciée par les insectes (Koptur, 2005). Deux sortes de nectars sont couramment décrites, le nectar floral (au niveau des fleurs) et le nectar extra-floral (provenant de nectaires situés en général le long de la tige) qui sont principalement constitué de sucres (sucrose, fructose, glucose) et d’un ensemble d’acides aminés variables selon les plantes (Blüthgen et al., 2004; Gardener and Gillman, 2001). Parmi ces acides aminés, la proline se retrouve couramment à des concentrations relativement élevées, aussi bien au niveau de la plante, lui permettant de lutter contre des stress abiotiques (sécheresse, hyper salinité) (Szabados and Savoure, 2010; Verslues and Sharma, 2010) qu’au niveau du nectar (Gardener and Gillman, 2001). Malgré une présence quasi-ubiquitaire au niveau des nectars floraux, couplée à son potentiel énergétique, décrit chez plusieurs espèces d’insectes (Bursell, 1981; Gäde and Auerswald, 2002; Sacktor, 1970; Teulier et al., soumis) le rôle potentiel de la proline comme «atout» pour attirer les insectes pollinisateurs n’a cependant été mis en exergue que récemment (Carter et al., 2006, Nepi et al., 2012). Le nectar extra-floral (NEF) joue quant à lui, un rôle majeur dans l’attraction de certaines espèces d’insectes non-pollinisateurs, tels que les fourmis (Ruffner and Clark, 1986) dont la présence permet de protéger la plante contre d’autres insectes herbivores (Katayama and Suzuki, 2004; Kost and Heil, 2005; Pulice and Packer, 2008). Ainsi, avec une vision finaliste, attirer un grand nombre de fourmis permettrait à la plante de limiter les dégâts engendrés par les insectes phytophages et donc d’améliorer sa fitness. Lanza et collaborateurs (Lanza, 1991; Lanza et al., 1993) ont montré que les fourmis de feu (genre Solenopsis) sont capables de choisir du nectar extra-floral comportant des acides aminés lorsque celui-ci est proposé face à du nectar sans acide aminé. Cependant la nature précise des acides aminés préférés n’a pas été recherchée. Plus récemment, il a été montré que certaines fourmis du genre Atta (fourmis coupeuses de feuille) étaient capables de détecter et de préférer des feuilles de plantes stressées dont la concentration en proline était plus élevée (Meyer et al., 2006; Ribeiro Neto et al., 2012). Le but de mon étude était de caractériser si la proline présente dans le NEF de Fallopia sp. pouvait être à l’origine d’un renforcement des interactions biotiques entre cette plante et une fourmi Lasius neglectus, deux espèces à fort pouvoir invasif. La première étape de ce projet, financée par la bourse de terrain de la SFE, était de vérifier expérimentalement, si les fourmis étaient capables de détecter la présence de proline en condition contrôlée, et de faire un choix face à plusieurs solutions sucrées, supplémentées ou non en proline.
Méthodes
Prélèvement et stabulation de la colonie de fourmis
Une partie d’une métacolonie de Lasius neglectus a été prélevée à Villeurbanne fin avril 2014 puis maintenue dans une caisse avec du substrat récolté au même moment pendant une semaine. Ensuite, la colonie a été répartie en 64 colonies composées de 500 individus environ et 3 reines et 5 cocons dans des boites en polypropylène de 33*19*11 cm (L*l*h) dont les parois verticales ont été préalablement recouverte d’une solution de téflon liquide, couramment utilisée par les entomologistes. Dans chaque boite, ont été placés deux tubes à essai remplis à moitié d’eau distillée, obturés par un coton et un carré de Parafilm pour éviter une évaporation trop importante. Les deux tubes à essai étaient ensuite recouverts d’un film plastique rouge, mimant un environnement adapté pour les fourmis. Cette boite représentait la « zone d’habitat » des sous-colonies. Les cycles jour/nuit étaient contrôlés (16h J/8h N).
Chaque boite a été percée pour laisser passer un tube PVC de 5 mm de diamètre interne et de 8 cm de longueur. Ce tube permettait le passage de la zone d’habitat à la zone expérimentale (voir descriptif ci-dessous).
Nourrissage
Chaque sous-colonie a été aléatoirement attribuée à différents protocoles de nourrissage pendant 4 semaines au minimum :
1) Nourries avec une solution sucrée (Glucose 10%)
2) Nourries avec une solution sucrée + proline (Glucose 10% + Proline 10mM)
3) Nourries avec une solution sucrée + alanine (Glucose 10% + Alanine 10 mM)
Suite à ce nourrissage, chaque colonie a subit une période de jeûne de 1 semaine pour stimuler leur effort de fourragement.
Protocole expérimental
1- Test de choix entre deux solutions
Les tests ont été effectués début juin dans une salle où l’apport de lumière était contrôlé et situé au-dessus du dispositif de choix.
Chaque colonie était testée une seule fois. Elles étaient confrontées à un choix entre deux solutions (Glucose 10% vs. Glucose 10% + Proline 10mM ou Glucose 10% vs. Glucose 10% + Alanine 10 mM ou Glucose 10% + Alanine 10 mM vs. Glucose 10% + Proline 10mM) réparties de façon aléatoire au cours des tests.
250 µL de chacune des solutions étaient placés dans un puits adapté pour que les fourmis n’aient aucune difficulté pour venir boire. Chaque réceptacle était disposé à 8 cm l’un de l’autre dans la zone expérimentale, constituée d’une boite en polypropylène de 16.5*19*9.5 cm (L*l*h), dont les parois ont été préalablement recouvertes de téflon liquide. Des caméras étaient disposées au-dessus de chaque zone expérimentale afin de suivre le nombre de fourmis fourrageuses.
Chaque test durait 90 min, durant lesquelles les fourmis avaient la possibilité de se diriger vers l’un ou l’autre des puits.
2- Paramètres pris en comptes
Après chaque test, les vidéos ont été analysées et toutes les 5 minutes, les fourmis qui étaient en contact avec les solutions ont été comptabilisées.
A la fin du test les fourmis ont été retirées de la zone expérimentale et le volume de solution restante a été mesurer pour estimer le volume bu pour chaque solution.
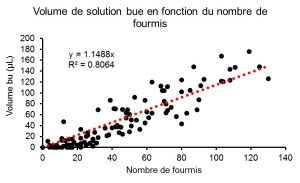
Ces deux paramètres sont fortement corrélés (Fig. 2), ce qui permet de valider le protocole de comptage.
De plus, afin de vérifier si les fourmis étaient réellement capables de faire un choix via notre protocole, 4 colonies ont subi aléatoirement le protocole de choix avec uniquement du glucose. Les fourmis ont choisi à 47% la cuve de gauche et à 53% la cuve de droite. Notre protocole est donc validé : les fourmis ne font pas de choix quand les solutions proposées sont identiques.
Résultats et discussion
Malgré une absence de significativité liée sans doute à un effectif trop faible (n=6-8), les résultats obtenus ont permis de dégager des tendances répondant en partie à nos hypothèses de départ.
Tout d’abord, les solutions enrichies en acides aminés attirent les fourmis nourries uniquement au glucose 10%. En effet, les fourmis choisissent à hauteur de 65% les solutions contenant de la proline (Fig. 3A) et à hauteur de 62% celles contenant de l’alanine (Fig. 3B).
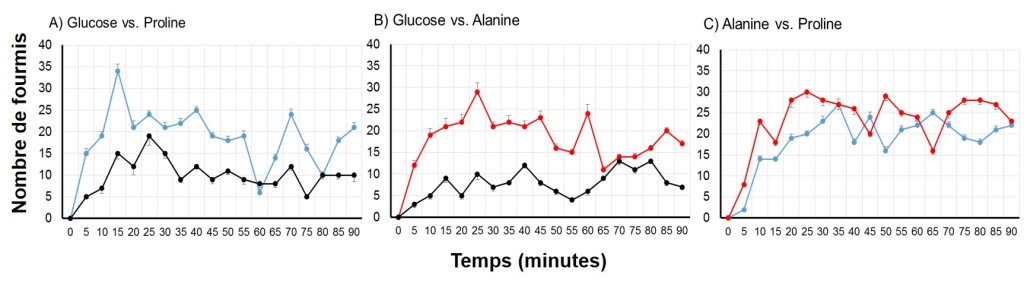
Figure 3 : Nombre de fourmis nourries au glucose 10% visitant chaque puits au cours du temps. A) Glucose (noir) vs. Proline (bleu), B) Glucose (noir) vs. Alanine (rouge), C) Alanine (rouge) vs. Proline (bleu).
Cette première tendance est en accord avec la littérature qui rapporte que les fourmis vont préférer une solution sucrée contenant plusieurs acides aminés. Cependant les protocoles précédents n’ont utilisé que des cocktails d’acides aminés. Notre but était alors de voir si les fourmis étaient capables de discriminer un peu plus finement la proline en particulier. D’après nos résultats, il semble que non : les fourmis ne font pas de choix lorsque les deux acides aminés sont proposés simultanément (Fig. 3C).
Cependant, si l’on se penche sur les résultats obtenus avec des fourmis nourries avec une solution de glucose enrichie soit en proline, soit en alanine, un comportement d’évitement a tendance à apparaitre. En effet, les fourmis habituées à la proline vont choisir à hauteur de 62% le glucose plutôt que la solution contenant de la proline (Fig. 4A). Quant aux fourmis élevées en présence d’alanine, elles vont choisir le glucose à hauteur de 73% (Fig. 4B).
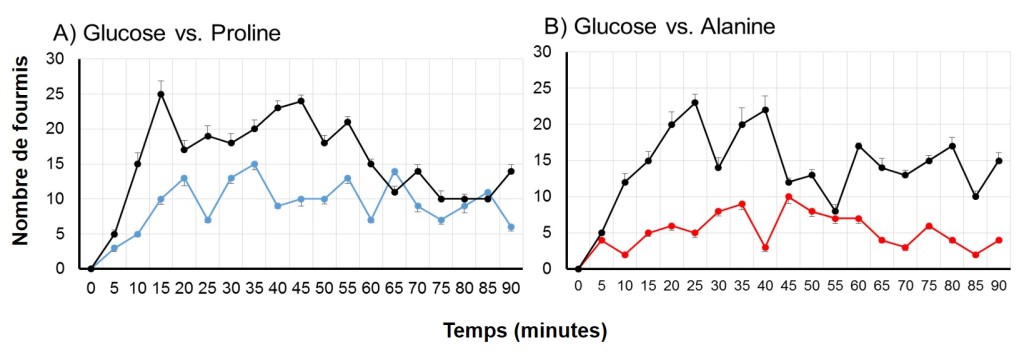
Figure 4 : Nombre de fourmis nourries soit au glucose + proline (A) soit au glucose + alanine (B) visitant chaque puits contenant de la solution de glucose 10% (trace noire) enrichie en proline (trace bleue) ou en alanine (trace rouge) au cours du temps
Ces résultats permettent de penser que les fourmis sont donc capables de sélectionner les acides aminés de façon très spécifique. Il semble ainsi que leur choix soit conduit par par la nouveauté : en effet, les fourmis élevées à l’alanine vont avoir tendance à choisir la proline à hauteur de 60% face à du glucose. Mais il apparait également que la nature des acides aminés entre en jeu lors du choix, puisque les fourmis élevées à la proline vont préférer le glucose à l’alanine lorsque ce choix leur est proposé (66%). Cette partie des résultats devrait être complétée par d’autres tests afin de dégager formellement une conclusion solide.
Pour conclure cette étude, nos résultats montrent que les fourmis ont tendance à choisir les solutions enrichies en acides aminés et sont capable d’ajuster leurs apports nutritifs en fonction de l’abondance de certains acides aminés dans leur quotidien.
En perspective, outre le fait d’améliorer la puissance statistique en augmentant le nombre de colonies testées, il serait très intéressant de réaliser des tests de choix en utilisant du nectar extra-floral de Fallopia afin de vérifier l’attractivité de ce nectar. A plus long terme, des expériences supplémentaires sur la bioénergétique des fourmis devraient permettre de vérifier si les fourmis sont capables d’utiliser la proline comme substrat énergétique, ce qui pourrait donc diriger leur choix vers des nectars à forte teneur en proline.
Remerciements
Cette étude n’aurait jamais pu se réaliser sans le soutien du laboratoire d’Ecologie des Hydrosystèmes Naturels et Anthropisés, qui m’a hébergé pendant cette période. Pour cela, Je souhaite remercier le Pr. Pierre Joly en qualité de directeur du LEHNA et le Pr. Yann Voituron en tant que directeur de l’équipe E2C (Ecophysiologie, Comportement, Conservation). Ensuite je voudrais remercier les Dr. Florence Piola (EVZH, LEHNA) et Bernard Kaufmann (E2C, LEHNA), qui m’ont apporté de nombreux conseils et prêté du matériel ainsi que le Dr. Jérôme Prunier (Post-doc, CNRS USR 2936) pour son aide en statistique. Enfin, je voudrai remercier plus particulièrement Jérôme Gippet, doctorant de l’équipe E2C, qui m’a aidé dans toutes les étapes du protocole.
Bibliographie
Blüthgen, N., Gottsberger, G. and Fiedler, K. (2004). Sugar and amino acid composition of ant-attended nectar and honeydew sources from an Australian rainforest. Austral Ecology 29, 418-429.
Bursell, E. (1981). The Role of Proline in Energy Metabolism. In Energy Metabolism in Insects, (ed. R. H. Downer), pp. 135-154: Springer US.
Carter, C., Shafir, S., Yehonatan, L., Palmer, R. G. and Thornburg, R. (2006). A novel role for proline in plant floral nectars. Naturwissenschaften 93, 72-79.
Gäde, G. and Auerswald, L. (2002). Beetles’ choice–proline for energy output: control by AKHs. Comparative Biochemistry and Physiology Part B: Biochemistry and Molecular Biology 132, 117-129.
Gardener, M. C. and Gillman, M. R. (2001). Analyzing variability in nectar amino acids: Composition is less variable than concentration. Journal of Chemical Ecology 27, 2545-2558.
Katayama, N. and Suzuki, N. (2004). Role of extrafloral nectaries of Vicia faba in attraction of ants and herbivore exclusion by ants. Entomological Science 7, 119-124.
Kawano, S., Azuma, H., Ito, M. and Suzuki, K. (1999). Extrafloral nectaries and chemical signals of Fallopia japonica and Fallopia sachalinensis (Polygonaceae), and their roles as defense systems against insect herbivory. Plant Species Biology 14, 167-178.
Koptur, S. (2005). Nectar as fuel for plant protectors. In Plant-provided food for carnivorous insects: a protective mutualism and its applications, (ed. P. C. J. v. R. F. L. Wäckers, J. Bruin), pp. 75-108.
Kost, C. and Heil, M. (2005). Increased availability of extrafloral nectar reduces herbivory in Lima bean plants (Phaseolus lunatus., Fabaceae). Basic and Applied Ecology 6, 237-248.
Lanza, J. (1991). Response of fire ants (Formicidae: Solenopsis invicta and S.gerninata) to artificial nectars with amino acids. Ecological Entomology 16, 203-210.
Lanza, J., Vargo, E. L., Pulim, S. and Chang, Y. Z. (1993). Preferences of the Fire Ants Solenopsis invicta and S. geminata (Hymenoptera: Formicidae) for Amino Acid and Sugar Components of Extrafloral Nectars. Environmental Entomology 22, 411-417.
Meyer, S. T., Roces, F. and Wirth, R. (2006). Selecting the drought stressed: effects of plant stress on intraspecific and within-plant herbivory patterns of the leaf-cutting ant Atta colombica. Functional Ecology 20, 973-981.
Nepi, M., Soligo, C., Nocentini, D., Abate, M., Guarnieri, M., Cai, G., Bini, L., Puglia, M., Bianchi, L. and Pacini, E. (2012). Amino acids and protein profile in floral nectar: Much more than a simple reward. Flora-Morphology, Distribution, Functional Ecology of Plants.
Pulice, C. E. and Packer, A. A. (2008). Simulated herbivory induces extrafloral nectary production in Prunus avium. Functional Ecology 22, 801-807.
Ribeiro Neto, J. D., Pinho, B. X., Meyer, S. T., Wirth, R. and Leal, I. R. (2012). Drought stress drives intraspecific choice of food plants by Atta leaf-cutting ants. Entomologia Experimentalis et Applicata 144, 209-215.
Ruffner, G. A. and Clark, W. D. (1986). Extrafloral Nectar of Ferocactus-Acanthodes (Cactaceae) – Composition and Its Importance to Ants. American journal of botany 73, 185-189.
Sacktor, B. (1970). Regulation of Intermediary Metabolism, with Special Reference to the Control Mechanisms in Insect Flight Muscle. In Advances in Insect Physiology, vol. Volume 7 eds. J. E. T. J.W.L. Beament and V. B. Wigglesworth), pp. 267-347: Academic Press.
Szabados, L. and Savoure, A. (2010). Proline: a multifunctional amino acid. Trends Plant Sci 15, 89-97.
Teulier, L., Weber, J.-M., Crevier, J., and Darveau, C.-A., Proline as a fuel for insect flight: Enhancing carbohydrate oxidation in hymenopterans. Submitted in Proc. R. B.
Verslues, P. E. and Sharma, S. (2010). Proline metabolism and its implications for plant-environment interaction. The Arabidopsis Book/American Society of Plant Biologists 8.



Commentaires récents