La Société Française d’Ecologie et Evolution (SFE2) vous propose ce ‘regard’ en deux parties d’Anne Teyssèdre, écologue et médiatrice scientifique, sur les réponses des espèces et communautés écologiques aux changements globaux (R80a), avec un zoom sur la dynamique des communautés de mammifères (R80b).
Une version plus courte de ce double article a été publiée en juillet 2018 par la revue L’Ecologiste (n°52), partenaire de publication de ces Regards sur la biodiversité. Une version actualisée, augmentée de plusieurs focus (foci), est parue dans l’Encyclopédie de l’Environnement en février 2021.
MERCI DE PARTICIPER à ces regards et débats sur la biodiversité en postant vos commentaires et questions sur les forums de discussion qui suivent les articles; les auteurs vous répondront.
———-
R80a : Quelles réponses des espèces et communautés aux changements globaux ?
- Introduction
- Les ressorts de l’adaptation des espèces au changement
- Largeur de niche et plasticité ‘phénotypique’
- Evénements catastrophiques et stratégies démogénétiques
- Potentiel d’adaptation et changements globaux
- Quelles principales réponses des espèces ?
- Encart 1 : Adaptations à l’anthropisation des habitats
- Encart 2 : Adaptations au changement climatique
- Quelle dynamique des communautés et réseaux écologiques ?
- Glossaire
- Bibliographie
- Regards connexes
R80b : Les mammifères face aux changements globaux
- Espèces menacées
- Les points faibles des grands mammifères
- Biais d’extinction au Quaternaire supérieur
- Accaparement des ressources et forçage des communautés
- Bibliographie et regards connexes
Forum de discussion sur ces regards R80a et R80b
—-
R80a : Quelles réponses des espèces et communautés écologiques
aux changements globaux ?
par Anne Teyssèdre
Docteure en biologie évolutive, auteure et médiatrice scientifique en écologie et sciences de l’environnement ( http://anne.teyssedre.free.fr/ )
Article édité par Sébastien Barot
——-
Mots clés : pressions humaines (anthropiques), changements globaux, espèces, potentiel adaptatif, niche écologique, plasticité individuelle (phénotypique), dynamique des populations, stratégie démogénétique, dynamique des communautés, adaptation, évolution.
——–
Introduction
Déforestation, fragmentation et pollution des habitats, intensification de l’agriculture et de l’élevage, urbanisation, modification et dérégulation du climat, acidification des océans, pêche industrielle intensive et peu sélective, transports d’espèces entre provinces biogéographiques… Notre espèce en expansion exerce par ses multiples activités des pressions croissantes sur les écosystèmes de la Planète. Comment les espèces et communautés* écologiques réagissent-elles à ces pressions ? Peut-on prévoir peu ou prou leurs dynamiques ?
Etant donné la diversité des changements environnementaux d’origine humaine (ou ‘anthropique’) et la multiplicité des espèces actuelles, qui se comptent en millions, il s’agira ici d’identifier les principaux ressorts de l’adaptation des espèces et communautés* aux changements environnementaux, et de les prendre en compte pour comprendre et anticiper les dynamiques en cours.
Dans un premier temps, nous explorerons le ‘potentiel d’adaptation’ des espèces aux changements environnementaux, à l’échelle des individus et des populations, pour en comprendre les déterminants et anticiper dans leurs grandes lignes les réponses des espèces aux changements en cours. Puis, prenant en compte plus explicitement les interactions entre espèces et les contraintes imposées aux communautés* et réseaux écologiques* par les activités humaines, nous évoquerons brièvement la dynamique et l’évolution de ces communautés et réseaux, ainsi que les risques et enjeux associés.
Les ressorts de l’adaptation des espèces au changement
Sur quoi s’appuie –et comment se construit- le « potentiel d’adaptation au changement » des espèces ? On sait depuis Darwin que celles-ci évoluent et se transforment au fil du temps sous l’action de la sélection naturelle, qui trie au sein des populations composées de multiples individus, dotés chacun de caractères biologiques en partie héritables, les individus les plus aptes à se reproduire, ou plus exactement à transmettre (avec leurs gènes) leurs caractéristiques individuelles aux nouvelles générations… Ce processus d’évolution et adaptation, orienté par la sélection naturelle, arme les espèces contre les variations habituelles de leurs conditions de vie à différentes échelles temporelles.
De façon plus explicite, les recherches en écologie et évolution confirment depuis soixante ans que les espèces sont adaptées à la variabilité des conditions de vie habituellement rencontrées par les individus, d’une part, mais aussi à la fréquence relative des événements de type catastrophique (i.e. infligeant une forte mortalité) rencontrés par les populations. Voyons comment.
Largeur de niche et plasticité ‘phénotypique’
Selon Hutchinson (1957), toute espèce ou population peut être caractérisée par sa « niche écologique », définie comme l’ensemble de ses exigences physiques, chimiques et biologiques -plus ou moins strictes- à un instant donné. Produits de la sélection naturelle, cette niche et ces exigences écologiques évoluent au fil des générations, avec la physiologie et le comportement des espèces. Elles reflètent la gamme et les variations des conditions environnementales auxquelles les individus sont couramment confrontés au cours de leur vie (et auxquelles ils participent), depuis plusieurs générations. En d’autres termes, la largeur de la niche écologique de chaque espèce, sa tolérance aux variations de température par exemple, est adaptée aux variations des conditions de vie habituellement rencontrées par les individus, dans le temps et dans l’espace.
Ainsi, les espèces habituellement exposées à des conditions écologiques variables, aux échelles spatiales et temporelles des individus, se sont adaptées à cette variation ; leur niche écologique en est élargie. Leur stratégie écologique est dite généraliste pour les paramètres ou ressources concernées. A l’inverse, les espèces exposées à des conditions de vie peu variables dans le temps ou dans l’espace, à l’échelle de plusieurs générations, se sont spécialisées à ces conditions. Les espèces de poissons et d’invertébrés pélagiques (i.e. de pleine mer), par exemple, sont généralement sténohalines* parce que la salinité de l’eau au large du littoral varie très peu (autour de 32°/°°); les espèces des estuaires en revanche sont nécessairement euryhalines*, car adaptées à de larges fluctuations de salinité.
La sélection naturelle prépare en outre les individus aux variations habituelles de leurs conditions de vie, durables ou récurrentes, en favorisant les modifications morphologiques, physiologiques ou/et comportementales adaptées à ces variations. Les individus font alors preuve d’une certaine plasticité dite ‘phénotypique’, qui peut être limitée aux étapes de développement (et donc être irréversible), ou bien se poursuivre tout au long de la vie, accompagnant les variations de l’environnement.
Parmi les adaptations phénotypiques irréversibles, citons la formation d’un casque protecteur chez les daphnies, conditionnée par la présence de poissons prédateurs dans leur habitat initial; ou le déterminisme de la caste chez les insectes sociaux (abeilles sociales, fourmis, termites, ..), dont les larves deviennent ouvrier(e)s, soldats (chez les termites) ou reproducteurs selon le régime alimentaire que leur administrent les ouvrier(e)s de la colonie.

Ecureuil roux et feuilles mortes…
(Cliché Pawel Ryszawa, CC BY-SA 3.0)
Lorsque les variations de l’environnement sont récurrentes ou cycliques, la plasticité des individus peut être réversible. La sélection naturelle prépare ainsi les individus aux variations saisonnières de leurs conditions de vie, ainsi qu’à l’alternance du jour et de la nuit (cycle nychtéméral). Dans les régions tempérées par exemple, à la fin de l’été, les arbres à feuilles caduques –sensibles au raccourcissement rapide de la longueur des jours, ou photopériode*- produisent des bourgeons (ébauches encapsulées de branches, feuilles ou fleurs), puis perdent leurs feuilles en automne et entrent en dormance pour l’hiver, accompagnant en cela maintes espèces animales – insectes, rongeurs..- qui se réfugient dans un abri pour hiverner ou hiberner, selon l’espèce. Plus actifs quand à eux, certains oiseaux tels que geais et casse-noix font des réserves de graines pour l’hiver, tandis que d’autres (insectivores notamment, telles nos fameux martinets et hirondelles) font provision de ‘carburant’ (graisse abdominale et thoracique) et migrent vers des latitudes plus clémentes, avant de revenir nicher à la belle saison.
Les organismes cependant ne sont pas de simples automates, programmés pour s’alimenter, se défendre et se reproduire dans un environnement aux variations prévisibles et contrôlées : la plupart sont également capables de réagir à des variations inattendues/imprévisibles de l’environnement par un comportement adéquat, révélant une certaine plasticité comportementale.
Moins inertes qu’on le pense souvent, les plantes ne sont pas en reste. Les végétaux peuvent ainsi réagir aux variations quotidiennes, non seulement cycliques (intensité lumineuse, température…) mais aussi imprévisibles (prédation des feuilles par herbivores/phytophages, infection par virus, compétition spatiale, …) de leur environnement local par des comportements adaptés, comme l’orientation ou/et l’ouverture des fleurs en fonction de leur exposition et de l’éclairage local, la synthèse de composés toxiques pour leurs prédateurs, l’émission de phéromones attractives pour des espèces alliées (telles que les parasites de leurs prédateurs) ou encore celle de phéromones d’alarme destinées aux plantes voisines de la même espèce, en cas d’agression.
Si elle existe chez les plantes, dénuées de véritables organes des sens (sans parler de centres d’analyse et de décision), la plasticité comportementale est une propriété générale des animaux, qui augmente avec leurs capacités d’apprentissage (capacités cognitives et pratiques), ainsi qu’avec leur socialité (complexité des groupes sociaux) et leur mobilité. Très appréciable chez certains invertébrés sociaux (ex: Abeille domestique) ou non sociaux (ex: Poulpe commun), elle culmine chez les mammifères et les oiseaux, dotés quant à eux de grandes capacités cognitives, de besoins énergétiques élevés et de systèmes sociaux souvent complexes (cf. par exemple Teyssèdre 2006).
Tolérance physiologique (homéostasie), ajustements morphologiques ou physiologiques et souplesse comportementale (dont capacités d’apprentissage et mobilité active) sont trois mécanismes permettant aux individus de réagir de manière adaptée aux variations habituelles de leur environnement local (via leur plasticité phénotypique). Comme tels, ces mécanismes contribuent au potentiel d’adaptation des espèces, face aux actuels changements globaux.
Evénements catastrophiques et stratégies démogénétiques
A une échelle de temps plus large, couvrant plusieurs générations, les caractéristiques biologiques (dites ‘traits de vie’) des espèces peuvent aussi évoluer en réponse à l’intensité des fluctuations de l’environnement imprévisibles à l’échelle des individus. Les recherches en écologie évolutive confirment depuis les travaux pionniers de Mac Arthur et Wilson (1967) dans ce domaine que les ‘stratégies démographiques’ des espèces sont adaptées à la fréquence relative des événements de type catastrophique, infligeant une forte mortalité aux populations.
Selon l’ampleur et la prévisibilité des changements environnementaux, étalés sur plusieurs générations, on peut schématiquement distinguer deux stratégies démographiques (ou plus exactement démogénétiques, voir plus bas) opposées, ou extrêmes : l’une de multiplication rapide des individus (dite ‘r’, pour reproduction) et de dispersion au hasard entre populations soumises à de grandes fluctuations de leurs effectifs, dans des habitats temporaires imprévisibles à l’échelle des individus ; l’autre de reproduction tardive et limitée mais compétitive (dite ‘K’), dans des habitats plus prévisibles et saturés.
Selon Pianka (1970), les principaux traits de vie favorisés par la sélection de type ‘r‘ sont : i) reproduction à un âge précoce, associée à courte durée de vie et à petite taille, ii) fécondité élevée, iii) dispersion précoce des ‘propagules’ (graines, œufs, larves…), par mobilité passive ou active. Et les traits de vie associés à la stratégie ‘K’ sont : i) reproduction tardive, corrélée à longue durée de vie (et à grande taille), ii) faible fécondité, iii) soins aux juvéniles, chez les animaux. [Voir cependant Reznick et al. 2002, Beaumont et al. 2009 ou Botero et al. 2015, pour une mise en perspective de ce modèle très simple.]
Toutes choses égales par ailleurs, la diversité génétique d’une espèce (ou méta-population*) augmente avec son abondance totale, en nombre d’individus. Elle augmente donc avec le taux de croissance (intrinsèque*) des populations, qui varie lui-même en sens inverse de l’âge de reproduction et de la taille des individus. C’est pourquoi, associé au hasard des migrations et des mutations génétiques, le taux de croissance intrinsèque* élevé des espèces prolifiques de petite taille (de type ‘r’) augmente non seulement leur capacité de résilience après décimation, au plan démographique, mais aussi accélère leur évolution et adaptation génétique face aux changements directionnels de l’environnement. La diversité génétique des nombreux ‘propagules’ et la brièveté des générations favorisent ainsi l’adaptation rapide de ces espèces aux changements directionnels de leur environnement, tels qu’une augmentation progressive de la température ou de la salinité des sols, par exemple. C’est pourquoi nous parlons ici de stratégie ‘démogénétique’.
Tirant parti de la fécondité et de la mobilité des individus, plutôt que de leurs adaptations et compétences en termes de survie locale, la stratégie ‘r’ (de multiplication rapide et dispersion) permet aux petites espèces prolifiques de rebondir après décimation locale. C’est la stratégie habituelle des microorganismes -tels que bactéries, protistes, champignons…- peuplant des habitats temporaires (hôtes animaux ou végétaux, habitats saisonniers, déchets organiques..), ainsi que des algues et champignons macroscopiques, aptes à coloniser rapidement tout nouvel habitat temporaire favorable.
Chez les végétaux (embryophytes), cette stratégie ‘r’ de multiplication et dispersion au hasard est celle de nombreuses plantes annuelles et graminées, qui dispersent en quantités pollens et graines sur de bonnes distances (via le vent ou le transport animal) et colonisent rapidement les habitats ouverts avant d’être broutées, piétinées, brûlées, fanées ou remplacées par d’autres espèces plus compétitives et longévives.

Estran. Comme la plupart des ‘invertébrés’ marins, les moules, bigorneaux, seiches et cirripèdes sont des espèces de types ‘r‘, très fécondes. (Cliché A. Teyssèdre)
Chez les animaux, elle constitue un atout pour la plupart des insectes et autres « invertébrés » à fécondité élevée et grandes capacités de dispersion des adultes ou des larves (dont la plupart des mollusques et crustacés), ainsi que dans une moindre mesure pour les poissons, dotés souvent d’une grande fécondité (mais voir plus bas). Moins radicale chez les oiseaux et mammifères, qui prodiguent tous des soins aux jeunes et donc dont les femelles ont une fécondité limitée, la stratégie ‘r’ de multiplication rapide caractérise cependant quelques ordres et familles (nombreuses) de petits mammifères soumis à d’amples fluctuations de leurs effectifs, tels que les rongeurs (souris, campagnols, lemmings, …).
Cette capacité de résilience et d’évolution rapide des populations, qui augmente avec leur taux de croissance intrinsèque* et leur diversité génétique, paraît un point fort des microorganismes et autres espèces prolifiques face aux actuels changements globaux. [C’est ainsi qu’apparaissent épisodiquement, puis prospèrent allègrement, des souches bactériennes résistantes à certains antibiotiques, des lignées de champignons résistantes aux antifongiques (e.g., rouille du blé, fusariose du maïs…), de plantes messicoles résistantes à des herbicides, ou d’insectes ‘ravageurs’ résistants à des insecticides.]
La stratégie démogénétique inverse (dite ‘K’) des mammifères longévifs et peu féconds, tels que les ongulés (cerfs, antilopes, rhinocéros, hippopotames…), les mammifères marins (baleines et dauphins, phoques et otaries) et les grands singes, qui élèvent au mieux un petit par an au sein de populations relativement restreintes (faible diversité génétique), les pénalise en revanche face aux bouleversements actuels de leurs conditions de vie (voir aussi le regard n°45 de J-L. Lebreton).
Soulignons cependant que la fécondité des femelles -et donc la stratégie démogénétique des espèces- varie, entre autres facteurs, avec l’ampleur des soins qu’elles peuvent prodiguer à leur progéniture ; elle varie donc avec la capacité des femelles (ou celle des hermaphrodites, chez les végétaux) à investir du temps et de l’énergie dans la survie et la reproduction de chacun de leurs rejetons. A défaut de soins parentaux, la sélection naturelle favorise les femelles les plus fécondes.
C’est ainsi que chez les végétaux, aux capacités parentales restreintes (du fait de l’immobilité des adultes reproducteurs), la stratégie démogénétique (K’) des grandes espèces longévives que sont les arbres, adaptés aux habitas (relativement) stables et saturés que sont les forêts, s’accompagne d’une bonne fécondité qui augmente avec la taille et donc l’âge des individus. De la même manière, peu capables de s’occuper des œufs qui se dispersent en mer lors du frai, les femelles des grandes espèces de poissons pélagiques tels que thons et cabillauds investissent dans le nombre (grande fécondité) et non pas dans la survie individuelle de leurs rejetons.
Potentiel d’adaptation et changements globaux
En bref, on peut distinguer trois grands facteurs d’adaptation des espèces aux changements de leur environnement, qui constituent trois dimensions de leur potentiel d’adaptation aux changements en cours : i) leur diversité génétique (ou encore leur abondance totale, en nombre d’individus), réservoir de diversité face aux changements imprévisibles de l’environnement, ii) leur taux de croissance ‘intrinsèque’ (c’est-à-dire le taux de croissance des petites populations), qui favorise leur résilience après décimation, et iii) la plasticité morphologique et comportementale des individus, dite plasticité phénotypique*.
Si les espèces prolifiques et de petite taille (de type ‘r’), dans l’ensemble des groupes systématiques*, réunissent généralement les deux premiers facteurs, le troisième caractérise notamment les espèces animales dotées de grandes capacités cognitives que sont les mammifères et oiseaux. Or ceux-ci sont pour partie des espèces ‘K’ de grande taille et peu fécondes, aux faibles effectifs, mal armées au plan ‘démogénétique’ pour affronter des changements amples et rapides de leur environnement. Dans ces conditions, peut-on prévoir la dynamique des espèces et communautés en réponse aux actuels changements globaux ?
Quelles principales réponses des espèces ?
Selon les caractéristiques biologiques et démographiques fondant le potentiel d’adaptation des espèces, on peut anticiper (et vérifier sur le terrain) :
- l’expansion d’espèces généralistes (‘r’ et ‘K’, dont la nôtre !), dans l’ensemble des écosystèmes modifiés par les activités humaines,
- la résilience d’espèces prolifiques de type ‘r’ (à grande fécondité, reproduction précoce, grande mobilité des « propagules » ou juvéniles), après décimation locale ou régionale,
- l’adaptation et l’évolution génétique rapide (voire la spéciation*) d’espèces ‘r’ confrontées à de nouvelles conditions de vie, dans les écosystèmes modifiés,
- l’adaptation comportementale et l’évolution génétique plus lente d’espèces ‘K’ généralistes ou commensales des humains, en expansion dans ces écosystèmes modifiées,
- le déplacement plus ou moins rapide d’espèces (‘r’ et ‘K’) vers des conditions de vie plus favorables, en réponse au réchauffement climatique (ex : déplacement vers les pôles ou en altitude),
- l’expansion et l’évolution génétique plus ou moins rapide (selon le type ‘r’ ou ‘K’) d’espèces domestiques et commensales des humains, dans les habitats anthropisés en expansion ;
mais aussi :
- le déclin et la disparition de nombreuses espèces ‘K’ spécialistes, fragilisées par la fragmentation et/ou la transformation progressive de leur habitat et incapables de rebondir après décimation locale,
- la raréfaction et disparition d’une fraction d’espèces ‘r’, notamment spécialistes, confrontées à la disparition ou transformation radicale de leurs habitats et ressources (ex : invertébrés et poissons des récifs coralliens, insectes en région d’agriculture intensive).
Attendues au plan théorique, ces diverses dynamiques sont observées sur le terrain (cf. encadrés 1 et 2), notamment chez les mammifères (voir le regard R80b, ci-dessous).
Encart 1 : Adaptations à l’anthropisation des habitats
Depuis plus de 50 ans, les « expériences » involontaires à vaste échelle de l’industrie et de l’agriculture confirment le potentiel d’adaptation génétique des espèces prolifiques (de type ‘r’) confrontées à l’anthropisation et à la modification chimique (pollution) de leurs habitats. Ainsi la résilience après décimation des populations de moustiques et leur adaptation (résistance génétique) au DDT, dans les années 1970, est bien connue ; l’adaptation génétique des ‘mauvaises herbes’ et autres plantes à fleurs à divers herbicides l’est plus encore, de même que celle des champignons parasites de plantes cultivées (tels la rouille du blé, le charbon du maïs, le cycloconium des oliviers…) aux fongicides, ou encore celle d’insectes phytophages (dont le Phylloxera de la vigne, la Pyrale du maïs, …) aux insecticides.
Plus récemment, des écologues ont mis en évidence l’adaptation génétique de populations de lombrics (Lumbricus rubellus) à la pollution des sols par les métaux. De la même manière, bien que moins résilientes et diversifiées que les populations de moustiques, des populations de poissons (tel le Choquemort Fundulus heteroclitus) se sont adaptées à la contamination de leur habitat par les PCB. [Cependant, le potentiel d’adaptation génétique des espèces très abondantes et fécondes aux changements de leurs conditions de vie, et en particulier à la pollution chimique de leurs habitats, n’est bien sûr pas illimité. Ainsi, le déclin d’espèces d’insectes pollinisateurs (abeilles et bourdons, papillons, coléoptères,..) observé dans les régions d’agriculture intensive depuis plusieurs décennies n’est pas uniquement le fait d’espèces spécialistes (e.g. Biesmeijer et al., 2006); il concerne aussi certaines espèces généralistes très abondantes avant la ‘révolution verte’, telles que l’Abeille domestique, dont les effectifs ont chuté de plus de 60% en 60 ans (Ellis, 2012) et dont les populations ne semblent pas près de s’adapter à la raréfaction des fleurs (plantes messicoles) qu’elles butinent ni à la toxicité croissante des pesticides systémiques (e.g. néonicotinoïdes) répandus dans les champs et vergers.]
Parmi les vertébrés, de nombreuses espèces de poissons ont réagi –génétiquement- à la pression de pêche par une reproduction plus précoce, qui permet aux adultes de passer entre les mailles du filet. Diverses espèces de passereaux, au taux de croissance démographique intrinsèque* relativement élevé, se sont adaptées à la vie en ville au plan génétique. Ainsi le chant des mésanges charbonnières a changé de fréquence, en réponse au bruit de fond du trafic urbain. Les merles noirs quant à eux se sont adaptés aux lumières artificielles nocturnes des villes par un moindre stress.

Goéland argenté urbain (Cliché A. Teyssèdre)
Rappelons par ailleurs que toutes les espèces d’oiseaux et de mammifères peuplant les villes et autres milieux anthropisés depuis des siècles s’y sont nécessairement adaptées (au moins) sur le plan comportemental, faisant preuve de grandes capacités d’innovation ou/et d’apprentissage par imitation. Parmi les espèces généralistes et mobiles faciles à observer, citons les goélands argentés et mouettes rieuses, deux espèces « d’oiseaux de mer » ubiquistes qui trouvent aujourd’hui leur pitance non seulement en prospectant le littoral à la recherche de petites proies et cadavres (petits crustacés, mollusques, poissons..), comme le faisaient leurs ancêtres, mais aussi en suivant les bateaux de pêche ou en les attendant au port pour se nourrir sur les quais des poissons rejetés, en capturant les lombrics émergés dans les champs à l’époque des labours, en inspectant les poubelles des villes et villages (à l’instar des chats, rats, chiens et renards) ou en se nourrissant de déchets organiques dans les décharges d’ordures…
Encart 2: Adaptations au changement climatique
En réponse au réchauffement global du climat, deux grands types d’adaptation sont attendus et observés, dans le monde tant animal que végétal (ex : Moritz et Agudo, 2013), que l’on peut voir comme deux dimensions, écologique et géographique (ou spatiale), de l’adaptation des espèces :
- Ajustement phénotypique* ou/et adaptation génétique de la niche écologique des individus et populations aux nouvelles conditions locales. C’est-à-dire : ajustement partiel du cycle de vie (phénologie) et d’autres caractéristiques biologiques (morphologie, physiologie) des individus et populations confrontés à de nouvelles conditions climatiques et écologiques locales (cycle des saisons, cycle nycthéméral), exploration et utilisation des micro-habitats et microclimats locaux, exploitation de nouvelles proies, confrontation et défenses contre nouveaux prédateurs et compétiteurs, etc.
- Déplacement de l’aire de répartition des populations vers des conditions climatiques plus favorables, c.à-d. principalement vers les pôles ou en altitude, avec une vitesse variable.
Les recherches et suivis de biodiversité des vingt dernières années documentent largement ces deux grands types de réponses, de la part des espèces comme des communautés. Au plan local, la plupart des plantes fleurissent et fructifient plus tôt au printemps dans les régions tempérées et boréales, avec un déphasage général du ‘verdissement’ des communautés végétales observé par satellite, à l’échelle des habitats, des paysages et des régions (ex : Bellard et al. 2011).

Citron et abeille sur pois de senteur
(Cliché A. Teyssèdre)
Les insectes répondent à ce déphasage en ajustant progressivement leur cycle de vie, via leur stratégie ‘r‘ ou/et leur plasticité comportementale, à celui des plantes dont ils se nourrissent. [C’est plus facile pour les espèces généralistes telles que les papillons citrons (Gonepteryx rhamni) et les abeilles (cf. photo ci-contre)… tant que les plantes ne sont pas arrosées de pesticides!] En outre, la couleur des ailes des papillons, libellules et autres insectes d’Europe s’éclaircit progressivement, à l’échelle régionale, en réponse à l’augmentation des températures estivales (Zeuss et al. 2014). La sélection naturelle en faveur d’une livrée plus pâle, absorbant moins les radiations solaires, joue en effet pour l’ensemble des espèces d’insectes sombres exposées à l’hyperthermie dans un climat plus chaud. [En d’autres termes, les populations d’espèces sombres se raréfient en Europe du Sud, mais elles évoluent aussi via la sélection et reproduction des individus les plus pâles.]
Mammifères, oiseaux et ‘reptiles’ s’adaptent localement plus ou moins bien, selon leur plasticité comportementale (et leur stratégie démogénétique), aux nouveaux cycles de vie de leurs proies et autres partenaires écologiques : déphasage des dates de migration ou d’hibernation, du calendrier de reproduction, utilisation de nouvelles ressources, …
Quant aux déplacements : à l’échelle de l’Europe, les communautés de plantes, de papillons et d’oiseaux suivies depuis plus de 20 ans étendent leur aire de répartition vers le Nord, à des vitesses variables selon les groupes et pays considérés (Devictor et al. 2012).
Ces réponses au changement climatique toutefois ne peuvent être que partiellement adaptatives (ex : Bellard et al., op.cit.). Elles semblent notamment insuffisantes pour inverser la dynamique de déclin des espèces spécialistes de type ‘K’ (i.e. longévives et peu fécondes), plus sensibles à la transformation et à la fragmentation massives de leurs habitats, pour plusieurs raisons :
- l’absence de synchronisation entre espèces, notamment selon leur niveau trophique, désorganise partiellement les réseaux écologiques* au détriment surtout des espèces spécialistes, longévives et peu fécondes (type ‘K’) ;
- étant donné la forme de la biosphère, des continents et du relief, la superficie des habitats au climat potentiellement favorable diminue vers les pôles et en altitude, limitant le nombre d’espèces ‘réfugiées climatiques’ (de type ‘r’ ou ‘K’) qui pourront s’y établir ; en outre, l’accessibilité de ces habitats n’est pas garantie, surtout pour les grandes espèces ‘K’ spécialistes (qui devront traverser des habitats défavorables ou/et anthropisés) ;
- toutes ces réponses ne peuvent protéger les populations d’espèces ‘K’ contre les effets dévastateurs d’événements climatiques extrêmes tels que sécheresses prolongées, tempêtes et inondations (voire typhons et tsunamis, en région tropicale), dont la fréquence augmente actuellement avec l’intensité du changement climatique.
Quelle dynamique des communautés et réseaux écologiques ?
A l’échelle des communautés écologiques, il est clair que l’expansion d’espèces généralistes aux dépens d’espèces spécialistes, dans l’ensemble des écosystèmes modifiés par les activités humaines, doit se traduire par une homogénéisation des faunes et flores régionales (McKinney et J.L. Lockwood 1999, Clavel et al. 2011) ainsi qu’un déclin du nombre total d’espèces à l’échelle mondiale [sauf diversification suffisante par spéciation* dans les habitats émergents isolés, cf. Thomas 2015].
Ainsi en Europe, en réponse à l’intensification de l’agriculture, les espèces d’oiseaux généralistes tels que mésanges charbonnières et mésanges bleues, étourneaux, corneilles noires et pigeons ramiers, qui fréquentent également les villes, villages, parcs et jardins, composent une fraction croissante de l’avifaune des champs, tandis qu’à l’inverse les oiseaux spécialistes des milieux agricoles tels que linottes mélodieuses, tariers des près, râles des genêts, huppes fasciées et vanneaux huppés se raréfient. Pour suivre cette dynamique de composition des communautés d’oiseaux, des chercheurs ont élaboré un index de spécialisation des communautés (moyenne pondérée des coefficients de spécialisation des espèces composant ces communautés), qui augmente avec la perturbation des habitats (Julliard et al. 2006) et confirme l’homogénéisation fonctionnelle des peuplements d’oiseaux de France depuis 20 ans (Clavel et al., op.cit., et regard n°16).
Mais ce n’est pas tout : formés de réseaux d’espèces coadaptées, évoluant en interaction entre elles et avec leur milieu physique depuis de nombreuses générations, les écosystèmes sont des systèmes organisés (et adaptatifs) complexes, de résistance et résilience limitées. La modification rapide de composition des communautés, jointe aux rythmes différents d’adaptation (génétique et phénotypique) des espèces aux changements de l’environnement, notamment du climat, désynchronisent et désorganisent ces réseaux, augmentant les risques de basculement vers un autre état stable, défavorable notamment aux humains (cf. Folke et al. 2004, Cardinale et al. 2012).
Sur l’ensemble du pourtour méditerranéen, par exemple, la surexploitation des forêts et le surpâturage local par le bétail (chèvres, moutons, vaches, buffles..) depuis plusieurs siècles a fait basculer nombre des écosystèmes locaux forestiers vers un état buissonneux (garigue, maquis) de faible évapotranspiration, donc piètres régulateurs du climat local, avec un risque accru de basculement vers la désertification par surpâturage et aridification du climat – accentué par le réchauffement climatique actuel global (voir le regard n°37 de Sonia Kefi). Cette dynamique de basculements successifs d’écosystèmes locaux vers un état stable de moindre productivité, complexité ou/et diversité trophique, nuit non seulement à de nombreuses espèces « non humaines » -notamment de mammifères et d’oiseaux- mais aussi aux populations humaines de ces régions.
Au fil du temps, les pressions sur les communautés et réseaux écologiques augmentent avec l’accaparement des terres et des ‘ressources’ par les sociétés humaines – via l’agriculture, la pêche, l’urbanisation, … De fait, la conversion ou dégradation d’habitats riches en biodiversité (tels que forêts, marais, rivières et mers poissonneuses..) en habitats appauvris (champs cultivés, rivières polluées, mers ‘surpêchées’), de moindre capacité biotique, réduit considérablement –au moins d’un quart, cf. Haberl et al. 2007- la quantité totale de ressources disponibles pour les espèces sauvages.

(Cliché A. Teyssèdre)
Cette restriction de ressources implique non seulement une réduction de l’abondance et de la biomasse des communautés animales et végétales concernées (ex : Gaston et al. 2004 ; Smil 2011), mais aussi du nombre d’espèces (ex : Teyssèdre et Couvet 2007, et voir ci-dessous le Regard associé (R80b) sur la dynamique des mammifères), et favorise un raccourcissement des réseaux trophiques (Pauly et al. 1998, Watson et Pauly 2005) avec un risque accru d’effondrement des écosystèmes.
En bref, le détournement et le raccourcissement des réseaux trophiques au ‘bénéfice’ des humains et de leurs espèces domestiques et commensales fragilise ces réseaux et le fonctionnement des écosystèmes, éventuellement jusqu’à leur basculement vers un autre état stable défavorable à quantité d’espèces dont la nôtre (e.g. Folke et al. 2004; Cardinale et al. 2012, et voir les regards n°30, n°31, n°37 et n°46). [Pensons aux océans surpêchés, acidifiés et pollués, qui se vident de leurs poissons et mammifères marins… au profit des méduses, plus que des humains !] Il est grand temps, pour nos sociétés dites modernes, de changer leur vision dominatrice et techniciste du monde et d’alléger leurs pressions sur les (socio)écosystèmes et la biodiversité…
Glossaire
- Communauté écologique, ou communauté biotique : Ensemble de populations d’espèces différentes, partageant certaines caractéristiques écologiques (souvent : espèces de même niveau trophique), occupant un même site ou une même région géographique. Exemples : Communauté de poissons ‘herbivores’ d’un lac alpin, communauté d’arbres d’une forêt tropicale, avifaune d’Europe.
- Démogénétiques (variables) : variables décrivant la structure et expliquant la dynamique d’une population ou espèce sur les plans tout à la fois démographique (effectifs des populations, structure d’âge, fécondité des femelles, taux de survie, taux de migration..) et génétique (diversité génétique, polymorphisme, liaisons entre allèles..).
- Groupe systématique : Ensemble d’espèces apparentées, issues d’un même ancêtre. Exemples : plantes à fleurs (angiospermes), insectes, mammifères, …
- Biotope: Habitat physique.
- Métapopulation : Ensemble de populations d’une même espèce, échangeant des migrants.
- Plasticité phénotypique: Variation des caractéristiques biologiques des individus (phénotype*) liée à leurs interactions avec leur environnement, et non pas à leurs gènes (génome, ou génotype).
- Phénotype : Ensemble des caractéristiques biologiques (morphologiques, physiologiques, écologiques, comportementales, …) d’un individu, donnant prise à la sélection naturelle.
- Réseau écologique : Réseau d’organismes (espèces) interdépendants, connectés par des relations de compétition, prédation, mutualisme, parasitisme, commensalisme, …, en interaction dans un même habitat ou biotope*.
- Spéciation: Formation d’une ou plusieurs espèces par différentiation génétique d’une ou plusieurs populations (ou sous-espèces) isolées au plan reproductif, soit par isolement géographique (spéciation allopatrique, ou parapatrique), soit par isolement écologique (spéciation sympatrique).
- Taux de croissance intrinsèque (d’une espèce) : Taux de croissance d’une population de cette espèce hors régulation densité-dépendante, c-à-d. sans compétition locale pour les ressources. C’est le taux de croissance d’une petite population de cette espèce, en expansion dans un habitat vacant.
Bibliographie
Beaumont H.J.E., J. Gallie et al., 2009. Experimental evolution of bet hedging. Nature 462 : 90-92.
Bellard C., C. Bertelsmeier, P. Leadley, W. Thuillier & F. Courchamp, 2012. Impacts of climate change on the future of biodiversity. Ecol. Lett. 15 : 365-377.
Biesmeijer J.C., Roberts S.P.M., Reemer, M. et al., 2006. Parallel declines in pollinators and insect-pollinated plants in Britain and the Netherlands. Science 313, 351–354.
Botero C.A., F.J. Weissing, J. Wright & D.R. Rubenstein, 2015. PNAS 112 : 184-189. Evolutionary tipping points in the capacity to adapt to environmental change.
Cardinale B. et al., 2012. Biodiversity loss and its impact on humanity. Nature 486 : 59-67.
Clavel J., Julliard R. and V. Devictor, 2010. Worldwide decline of specialist species : toward a global functional homogenization? Front. Ecol. Environ. 2 : 222-228.
Devictor V., C. van Swayy et al., 2012. Differences in the climatic debts of birds and butterflies at a continental scale. Nature Climate Change 2 : 121-124.
Ellis, J., 2012. The honey bee crisis. Outlooks Pest Manag. 23, 35–40.
Folke C., S. Carpenter et al., 2004. Regime shifts, resilience and biodiversity in ecosystem management. Ann. Rev. Ecol. Syst. 35 : 557-581.
Gaston K.J., T.M. Blackburn, K. Klein Goldewijk, 2003. Habitat conversion and global avian biodiversity loss, Proc. R. Soc. Lond. B 270 : 1293–1300.
Haberl H., 2007. Quantifying and mapping the human appropriationof net primary production in earth’s terrestrial ecosystems. P.N.A.S. 104 : 12944-12947.
Hutchinson GE. 1957. Concluding remarks. CoM Spring Harbor Symp Quant Biol 22: 415–27.
Julliard R., J. Clavel et al., 2006. Spatial segregation of bird specialists and generalists in bird communities. Ecol. Letters 9 : 1237–1244.
MacArthur R.H. & E.O. Wilson, 1967. The theory of island biogeography. Princeton Univ. Press, Princeton, NJ.
McKinney M.L. & J.L. Lockwood, 1999. Biotic homogenization : a few winners replacing many losers in the next mass extinction. T.R.E.E. 14 : 450-453.
Moritz C. & R. Agudo, 2013. The future of species under climate change : Resilience or decline ? Science 341 : 504-508.
Parmesan C., 2006. Ecological and evolutionay responses to recent climate change. Annu. Rev. Ecol. Syst. 37 : 637-669.
Pauly D, V. Christensen V, J. Dalsgaard J, R. Froese & F.S.B. Torres, 1998. Fishing down marine food webs. Science 279: 860-863.
Pianka E.R., 1970. On r and K selection. Am. Nat. 104 : 592-597.
Reznick D., M.J. Bryant & F. Bashey , 2002. R– and K-section revisited : The role of population regulation in life history evolution. Ecology 83(6) : 1509-1520.
Smil V., 2011. Harvesting the Biosphere : the Human Impact. Pop. Dev. Rev. 37(4) : 613-636.
Teyssèdre A., 2006. Les clés de la Communication animale. Delachaux et Niestlé, Paris.
Teyssèdre A. & D. Couvet, 2007. Expected impact of agriculture expansion on the world avifauna. C. R. Acad. Sci. Biol. 330 : 247-254.
Thomas C.D., 2015. Rapid acceleration of plant speciation during the Anthropocene. Trends Ecol. Evol. 30 : 448-455.
Watson R. & D. Pauly, 2001. Systematic distortions in world fisheries catch trends. Nature 414(6863): 534-536.
Zeuss D., R. Brandl et al., 2014. Global warming favours light-coloured insects in Europe. Nature Communications 5, 3874.
Regard associé :
Teyssèdre A., 2018. Les mammifères face aux changements globaux. Regards et débats sur la biodiversité, SFE, regard n°80b, juin 2018
—–
Regards connexes :
Barbault R. et A. Teyssèdre, 2013. Les humains face aux limites de la biosphère. Regards et débats sur la biodiversité, SFE, regard n°51, 23 novembre 2013.
Clavel J., 2011. L’homogénisation biotique, une réponse aux changements globaux. Regards et débats sur la biodiversité, SFE, regard n°16, 18 avril 2011.
Julliard R., 2011. Regards sur une perruche. Regards et débats sur la biodiversité, SFE, regard n°2, 11 octobre 2011
Julliard R. et F. Jiguet, 2011. Les oiseaux et la biodiversité face au changement climatique. Regards et débats sur la biodiversité, SFE, regard n°22, 11 octobre 2011.
Kéfi S., 2012. Des écosystèmes sur le fil : transitions catastrophiques. Regards et débats sur la biodiversité, SFE, regard n°37, 19 octobre 2012.
Lavorel S., R. Barbault et J.C. Hourcade, 2012. Impact et enjeux du changement climatique. Regards et débats sur la biodiversité, SFE, regard n°30, 3 avril 2012.
Lebreton J-D., 2013. Biodiversité et dynamique des populations. Regards et débats sur la biodiversité, SFE, regard n°45, 26 avril 2013.
Masson-Delmotte V., 2011. Le climat de notre biosphère. Regards et débats sur la biodiversité, SFE, Regard n°10, janvier 2011.
Pauly L. et F. Le Manach., 2012. Expansion et impact de la pêche mondiale. Regards et débats sur la biodiversité, SFE, regard n°31, 30 avril 2012.
Robert A., 2011. Les petites populations – Processus démographiques, génétiques et vortex d’extinction. Regards et débats sur la biodiversité, SFE, regard n°9, 10 janvier 2011.
Teyssèdre A., 2017. Le modèle IPAT et la transition écologique. Regards et débats sur la biodiversité, SFE, regard n°71, 15 avril 2017.
Thompson J. et O. Ronce. Fragmentation des habitats et dynamique de la biodiversité. Regards et débats sur la biodiversité, SFE, Regard n°6, 18 novembre 2010.
—
Article édité par Sébastien Barot, illustré et mis en ligne par Anne Teyssèdre.
R80b : Les mammifères face aux changements globaux
par Anne Teyssèdre
——-
Mots clés : mammifères, biogéographie, espèces menacées, dynamique des populations, dynamique des communautés, activités humaines, changements globaux, biais d’extinction, Quaternaire supérieur,
Holocène, Anthropocène.
——–
Selon l’Union Internationale pour la Conservation de la Nature (UICN, 2017), près d’un quart des espèces de mammifères connues au 20e siècle -soit 1219 espèces sur 5487- sont menacées d’extinction ou récemment disparues. Ou, plus exactement, plus d’un quart (26,2%) des 4651 espèces de mammifères dont le statut de conservation a pu être évalué, car suffisamment étudiées sur les plans biogéographique et démographique, sont menacées ou récemment disparues.
Espèces menacées
Ces espèces menacées ou récemment éteintes cependant ne constituent pas un échantillon au hasard des mammifères. Elles sont plus nombreuses parmi les espèces de grande taille, à reproduction tardive et peu fécondes (espèces dites ‘K’, voir le regard R80a associé), spécialistes d’habitats naturels ou semi-naturels, peu anthropisés. Ainsi, toutes les espèces (connues et évaluées au plan biogéographique) de moshidés (cerfs porte-musc), hippopotames et siréniens sont menacées d’extinction, de même qu’une large majorité des périssodactyles (13 espèces sur 16 d’équidés, rhinocéros et tapirs), des cervidés (26 sur 45 espèces) et des ours (6 sur 8 espèces). L’un des ordres les plus touchés est le nôtre, celui des primates, qui rassemble singes, humains, lémuriens et tarsiers : parmi les espèces suffisamment étudiées, tous les ‘grands singes’ (c-à-d. les chimpanzés communs et bonobos, gorilles et orang-outans), tous les gibbons et siamangs (16 espèces), la quasi totalité des lémurs et indris (28 espèces sur 32) sont menacées – notamment par la disparition de leur habitat forestier.
A l’opposé, moins de 20% des espèces connues et étudiées de chauves souris (183 sur 946 espèces étudiées) et de rongeurs (environ 400 sur 1900 espèces étudiées), ou encore 12% des opossums (9 sur 78 étudiées), espèces généralement de petite taille, sont considérées comme menacées d’extinction ou récemment éteintes.
Les points faibles des grands mammifères
Cette vulnérabilité supérieure des grands mammifères spécialistes a plusieurs explications, détaillées dans le regard associé. D’une part, face à la réduction, fragmentation et transformation massive des habitats, la spécialisation à des conditions de vie bien précises constitue bien sûr un handicap ; à l’inverse, l’eurytopie ou « stratégie généraliste » est un atout évident.

Rhinocéros blancs (ici en captivité), espèce quasi menacée selon l’UICN (Cliché A. Teyssèdre)
D’autre part, les mammifères de grande taille sont plus vulnérables parce que :
• espèces ‘à sang chaud’ (homéothermes) dotées d’un métabolisme et de besoins énergétiques élevés, leurs exigences spatiales augmentent avec leur taille et leur niveau trophique (des herbivores aux carnivores); de ce fait, dans leurs habitats fragmentés ou dégradés (par l’agriculture, l’urbanisation, le changement climatique..), les populations de grands mammifères sont souvent proches ou en deçà du seuil de viabilité (cf. le regard n°9 d’A. Robert) ;
• la viabilité des petite populations de grands mammifères est en outre réduite par leur faible taux de croissance intrinsèque*, dû à la maturité tardive et à la faible fécondité des femelles (voir le regard 80a associé, et le regard n°45 de J-D. Lebreton);
• espèces compétitrices ou proies pour les humains, ce sont les cibles privilégiées des chasseurs et braconniers ; à l’échelle des populations, la chasse ne réduit pas seulement les effectifs locaux (du fait de la faible fécondité des femelles) mais aussi l’intensité des échanges entre populations régionales (dans les habitats fragmentés), ce qui réduit la viabilité des métapopulations* (ensembles de populations échangeant des migrants) (cf. Theodorou et al. 2009).
Biais d’extinction au Quaternaire supérieur
Soulignée depuis les années 2000 (ex : Cardillo et al., 2005), la vulnérabilité des grands mammifères confrontés aux activités humaines et autres grands changements environnementaux ne date pas d’hier. Ainsi, Rodolfo Dirzo et ses collaborateurs (2014) ont estimé à 182 Kg le poids médian des espèces de mammifères disparues au Pléistocène supérieur, entre -120.000 et -10 000 ans. Il s’agit notamment des célèbres mammouths, rhinocéros laineux, ours, lions et autres grands carnivores des cavernes, pour l’Europe et l’Amérique du Nord – toutes espèces doublement menacées à la fin de la dernière glaciation, par les humains (prédation, compétition) et par le réchauffement climatique. Mais aussi de toutes les espèces de marsupiaux excédant 45 Kg qui peuplaient l’Australie avant sa colonisation par les humains, il y a quelque 50 000 ans, et qui ont disparu moins de 10 000 ans après, probablement victimes de la chasse et des feux de brousse, sans changement significatif du climat.
Dans un article récent, F.A. Smith et al. (2018) ont confirmé que l’important biais d’extinction de grands mammifères au Quaternaire supérieur, de -125.000 ans à aujourd’hui, est caractéristique de cette brève période géologique relativement à l’ensemble des 65 millions d’années couverts par l’Ere Cénozoïque (i.e. Tertiaire + Quaternaire), c’est-à-dire depuis la dernière crise majeure d’extinction, marquant la fin de l’Ere Mésozoïque (ou Secondaire). Sachant que les climats régionaux et le climat mondial ont largement varié au cours du Cénozoïque, notamment à la fin du Miocène et pendant les cycles de glaciation du Quaternaire, sans biais d’extinction ‘en faveur’ des grands mammifères jusqu’au Paléolithique moyen (début du Quaternaire supérieur) et avant les premières vagues de migrations d’humains hors d’Afrique, il y a 125.000 ans, il semble plus que probable que les humains sont responsables de ce ‘biais’. Selon cette étude, par ailleurs, notre espèce Homo sapiens n’est plus seule en cause : armés de lances et de pieux aux pointes durcies par le feu, les néanderthaliens Homo neandertalensis et peut-être les dénisoviens (Homo ? denisova) semblent également impliqués dans la disparition des grands mammifères d’Eurasie.
Après la décimation des grands mammifères du Pléistocène supérieur, tout d’abord en Eurasie et probablement en Afrique (à partir de – 120.000 ans, par H. sapiens et H. neandertalensis pour l’Eurasie), puis vers – 45.000 ans en Australie, puis vers – 13.000 ans dans les deux Amériques (du Nord et du Sud), les humains de l’Holocène et contemporains ont pris le relais, s’en prenant quant à eux nécessairement à des espèces terrestres de plus petite taille… ainsi qu’aux grands mammifères marins (cf. Schipper et al. 2008). Pour s’en tenir aux mammifères terrestres, Dirzo et al. (2014) estiment le poids médian des espèces récemment menacées ou éteintes à 500 grammes… et celui des espèces sauvages non menacées à 60 grammes ! [Ce résultat est plus facile à admettre si l’on se souvient que 70% des espèces actuelles de mammifères sont des rongeurs, chauves-souris et ‘insectivores’ (eulipotyphla) de petite taille.]

Rhinocéros laineux ‘immortalisé’ par un artiste aurignacien, il y a environ 35000 ans, dans la grotte Chauvet (CC – Bloody Libu)
Accaparement des ressources et forçage des réseaux écologiques
Explorant plus spécifiquement les impacts de l’agriculture et l’élevage sur la faune sauvage, dans un passé relativement récent, Vaclav Smil (2011) estime que la biomasse des mammifères sauvages a été divisée par deux au cours du 20e siècle, chutant de 10 millions de tonnes de Carbone (MtC) en 1900, à 5 MtC en 2000. Les grandes espèces surtout ont été affectées. Cette dynamique de déclin cependant ne peut être étendue à l’ensemble des grands mammifères, qui comprennent également les humains et leurs animaux domestiques.
De 1900 à 2000, tandis que la biomasse des mammifères sauvages chutait de 10 à 5 MtC, celle des humains augmentait de 13 à 55 MtC et celle des mammifères domestiques de 35 à 120 MtC -dont 80 MtC pour les seuls bovidés domestiques! L’expansion démographique de notre espèce, via l’expansion et l’intensification de l’agriculture, implique en effet l’accaparement par les humains d’une fraction croissante de la productivité primaire (biomasse végétale) des écosystèmes (Haberl et al. 2007), à la base des réseaux trophiques et plus largement écologiques, et donc le détournement de ces réseaux au ‘bénéfice’ des humains et d’une minorité d’espèces associées, domestiques et commensales. Détournement des réseaux écologiques qui non seulement prive d’habitats et de nourriture (organique et minérale) quantités d’espèces animales et végétales, mais aussi désorganise et fragilise l’ensemble des écosystèmes concernés. La disparition des grands mammifères sauvages est un symptôme de cette dynamique de crise.
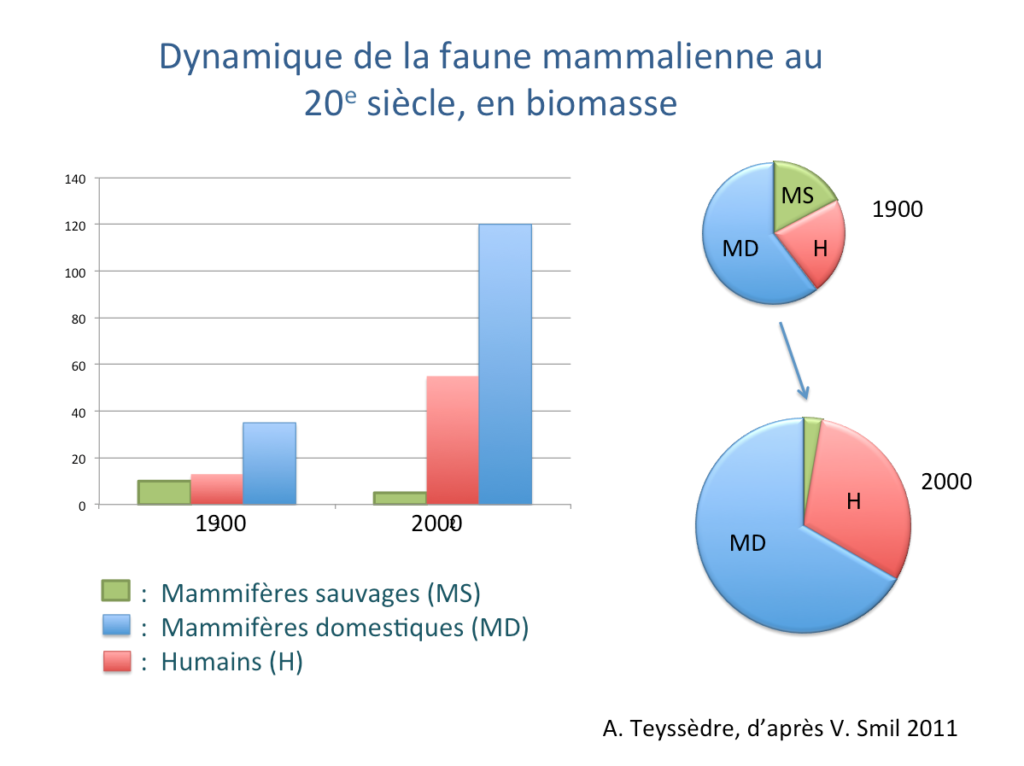
Variation de biomasse des mammifères au 20e siècle. A gauche, biomasses des mammifères sauvages, domestiques et humains en millions de tonnes d’équivalent Carbone (MtC). A droite, mêmes données en proportions de la biomasse totale des mammifères. (Schéma A. Teyssèdre d’après les estimations de V. Smil, 2011.)
[Si la biomasse totale des mammifères a été multipliée par trois en un siècle, c’est au ‘bénéfice’ des humains et aux dépens des espèces sauvages, en biomasse (-50%) comme en nombre d’espèces. Aujourd’hui, moins de 0,3% des espèces de mammifères – la nôtre et une douzaine d’espèces domestiques – représentent à elles seules 97% de la biomasse mammalienne.]
Bibliographie
Cardillo M., G.M. Mace et al., 2005. Multiple causes of high extinction risk in large mammal species Science 309 : 1239-1241.
Dirzo R., H.S. Young et al., 2014. Defaunation in the Anthropocene. Science 345 : 401-406.
Haberl H., 2007. Quantifying and mapping the human appropriationof net primary production in earth’s terrestrial ecosystems. P.N.A.S. 104 : 12944-12947.
Shipper J., J.S. Chanson et al., 2008. The status of the world’s land and marine mammals : diversity, threats and knowledge. Science 322 : 225-230.
Smil V., 2011. Harvesting the Biosphere : the Human Impact. Pop. Dev. Rev. 37(4) : 613-636.
Smith F.A., R.E. Elliot Smith, S.K. Lyons & J. Payne, 2018. Body size downgrading of mammals over the late Quartenary. Science 360 : 310-313.
Regard associé :
Teyssèdre A., 2018. Quelles réponses des espèces et des communautés écologiques aux changements globaux ? Regards et débats sur la biodiversité, SFE, regard n°80a, juin 2018.
Regards connexes :
Couvet D. et A. Teyssèdre, 2016. Quelle politique agricole pour le 21e siècle ? Regards et débats sur la biodiversité, SFE, Regard n°68, avril 2017.
Gheerbrandt E., 2010. La diversification des mammifères. Regards et débats sur la biodiversité, SFE, regard n°5, 8 novembre 2010.
Lebreton J-D., 2013. Biodiversité et dynamique des populations. Regards et débats sur la biodiversité, SFE, regard n°45, 26 avril 2013.
Merceron G. et A. Teyssèdre, 2012. Les Grands Singes du Miocène… et d’aujourd’hui. Regards et débats sur la biodiversité, SFE, regard n°40, 31 décembre 2012.
Patou-Mathis M. et C. Vercoutère, 2012. Ecologie et diversité des hommes du Paléolithique, Regards et débats sur la biodiversité, SFE, regard n°39 a et b, 3décembre 2012.
Pison G., 2012. Dynamique de la population mondiale. Regards et débats sur la biodiversité, SFE, Regard n°33, juin 2012.
Robert A., 2011. Les petites populations – Processus démographiques, génétiques et vortex d’extinction. Regards et débats sur la biodiversité, SFE, regard n°9, 10 janvier 2011.
Teyssèdre A., 2017. Le modèel IPAT et la transition écologique. Regards et débats sur la biodiversité, SFE, Regard n°71, avril 2017.
Thompson J. et O. Ronce, 2010. Fragmentation des habitats et dynamique de la biodiversité. Regards et débats sur la biodiversité, SFE, Regard n°6, 18 novembre 2010.
—
Article édité par Sébastien Barot, illustré et mis en ligne par Anne Teyssèdre.


Une excellente mise au point, claire et détaillée,sur un sujet d’actualité.
Pour information, j’ai publié il y a quelques années un article traitant du même problème: quelles sont les « stratégies » des espèces qui vont être favorisées ou défavorisées par les changements globaux actuels?
Pour le télécharger: https://www.researchgate.net/publication/236267524_Disturbances_organisms_and_ecosystems_a_global_change_perspective
Un test de l’hypothèse émise dans cet article a été effectué sur une famille d’oiseaux, les Fringillidae (pinsons): https://www.researchgate.net/publication/320560010_Ancestrality_and_evolution_of_trait_syndromes_in_finches_Fringillidae
Bonjour,
Ce regard de grande qualité, comme les autres, permet de comprendre les bases sur un sujet d’actualité.